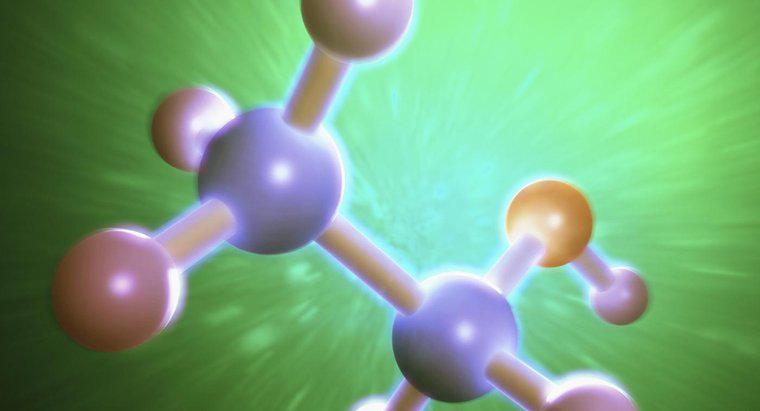
Üç moleküller arası etanol kuvveti vardır. Bunlar Londra dispersiyonu, dipol-dipol ve hidrojen bağıdır. Bu kuvvetlerin üçü de, oluşturdukları bağ türleri ve çeşitli bağ kuvvetleri nedeniyle farklıdır.
İlk kuvvet, Londra'nın dağılması, aynı zamanda en zayıf olanıdır. Londra dağılımında moleküller arası çekim her molekül arasında gerçekleşir. Bu, geçici olarak polarize olduklarında her molekül arasındaki elektron değişiminin sonucu olur. Bu geçici polarizasyon, molekülün bir tarafında elektron yoğunluğu diğerinden daha yüksek olduğunda meydana gelir.
Dipol-dipol çekiciliği, etanolün hem pozitif yüklü hem de negatif yüklü bir ucu olan polar bir molekül olması nedeniyle oluşur. Pozitif ve negatif yükler birbirlerine çekildiğinden, her bir molekülün zıt kutupları bağ oluşturur. Bu çekim Londra dağılımından daha güçlü, ancak üçüncü çekim türü olan hidrojen bağlarından daha zayıf.Son kuvvet, hidrojen bağıdır. Hidrojen bağları, proton moleküldeki oksijen elektronları çifti ile bağlandığında meydana gelir. Bu bağı sağlayan molekül donör olarak bilinirken, hidrojenin çekildiği elektronlara sahip olan molekül alıcı olarak bilinir. Etanol O-H bağını içerir, bu da bir hidrojen bağı oluşturmasını sağlar.