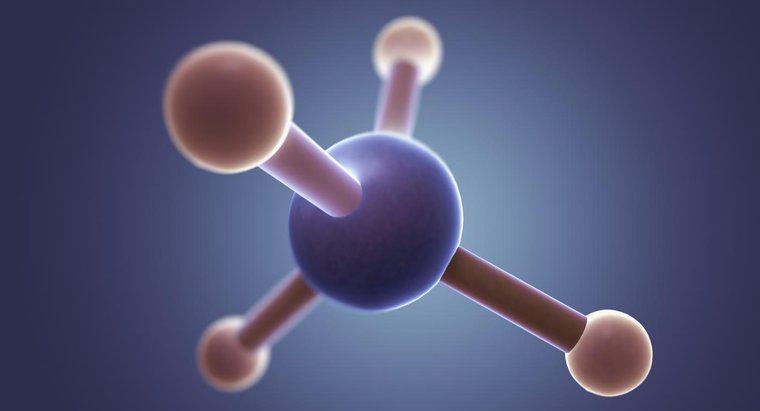
CH3Br için Lewis yapısı, etrafında dört elektron bulunan merkezdeki karbona sahiptir ve her biri karbon ile tek bir elektron paylaşan üç hidrojen ve bromdur. onu çevreleyen.
Lewis yapıları, atomların tam bir molekül oluşturmak için birbirlerine nasıl bağlandıklarını gösterir ve bromometan gibi temel moleküllerde bağlanma göstermek için faydalıdır. Bazı durumlarda çizgiler, bağları belirtmek için kullanılır, ancak bazik bileşiklerle uğraşırken noktalar daha yaygındır. Yapıştırma elektronlarına ek olarak, bu diyagramlar ayrıca bromometan içinde brom durumunda olduğu gibi yapışmayan elektronları da gösterir. Bromin, bu örnekte, karbon ile karbon arasındaki bağda aktif olarak yer almayan üç çift elektron vardır.
Genel olarak, Lewis yapıları, hidrojen dışındaki çoğu atomun dış kabukları içinde toplam sekiz elektron elde etmek için moleküller oluşturduğunu göstermektedir. Bununla birlikte, bu yapılar bir molekülün genel şeklini ima etmek için de kullanılabilir. Bromometan söz konusu olduğunda, karbon etrafındaki dört atomun 3B alanda oldukça düzgün bir şekilde düzenlenmesi gerekir, bu yüzden bir tetrahedral yapı oluştururlar. Bununla birlikte, brom bu kadar uzun (ve bu nedenle daha zayıf) bir bağ oluşturduğundan, hidrojenler metandan biraz daha fazla alana sahiptir, bu da hafifçe çarpık bir tetrahedral olur.