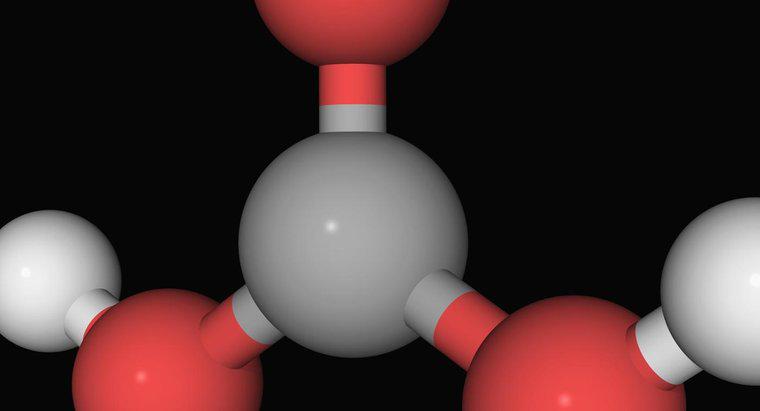
Karbonik asit oluşumu için dengeli denklem CO2 + H 2 OH 2 CO 2 H + + HCO < > 3- Karbonik asit, karbon dioksit veya CO 2 içerisinde su veya H 2 O çözünmesinden oluşur. p> Karbonik asit veya H 2 CO 3 , solunumda hayati bir rol oynayan zayıf bir asittir; ve içeceklerin karbonatlaştırılması. Sıvı bir çözeltide, karbonik asit kolayca yüklü bikarbonat iyonuna (HCO <3->) ve bir protona (H +) ayrışır. Hücrelerdeki metabolik işlemler sırasında CO2Sub> oluştuğunda, bir iyon olan bikarbonata dönüşür. Bu dönüşüm, bikarbonatın ekshalasyon için CO2'ye geri dönüştüğü kanda akciğerlere taşınmasını sağlar. Memelilerde, aynı işlem, karbonik asit üretimi ile karbon dioksit ve suya dönüşümü arasındaki reaksiyonu ileri geri hızlandırabilen bir enzim olan karbonik anhidraz ile gerçekleşir. Bikarbonat, trisiklik antidepresanlarda asidozu veya aşırı dozu tersine çevirmeyi denemek için kardiyopulmoner resüsitasyonda geçici bir önlem olarak, kanın pH'sini tamponlama kabiliyeti nedeniyle kullanılır. Solüsyonda çok fazla asit (H +) varsa, denge bikarbonatın (HCO <3- su>) karbonik asite (H
Benzer mesajlar
Diğer ilginç yazılar